|必读|FDA称Moderna疫苗有效且安全, 政府增购1亿剂
时间:2020-12-16

美国遍地都是C-O-V-I-D-M-R-N-A
上周五,FDA批准了辉瑞—BioNTech联合研发的mRNA新冠疫苗“紧急使用授权”(EUA)。
本周一,全美范围同时开始了大规模接种新冠疫苗,医学界同行谨慎称赞这是“疫情结束的开始!,不是疫情的结束。”
本周四(17日), FDA将根据Moderna提交申请新冠病毒mRNA疫苗"紧急应用授权"召开专家咨询评议研讨会。我们在第一时间获取了FDA内部专家审评报告和Moderna提交FDA的申请资料。
根据FDA疫苗审评专家提交的报告看,FDA认为该mRNA疫苗对18岁和以上成年人有效(辉瑞疫苗接种范围是16岁及以上)。
FDA审评专家在报告中没有对该疫苗提出特别关注的安全问题(辉瑞疫苗提及有过敏症患者慎用或暂且不用)。FDA请求专家咨询委员会审议批准Moderna新冠疫苗获"紧急使用授权"。
另据路透社报道,美国政府已确定再增购1亿剂Moderna新冠疫苗,这是最初预定购量的两倍(共32亿美元订单),希望确保明年6月底之前保障民众都有机会接种新冠疫苗。与此同时,辉瑞仍在和政府谈判是否明年增加供货一亿剂疫苗。由此可见在未来几个月内,新冠疫苗的供货将出现稳定状态。
根据业界人士推测,这两种疫苗以及随后其他新冠疫苗获得EUA授权后,将出现明确对比,不仅仅是预防感染保护作用,更多人将密切关注接种疫苗后不良反应或长期保护效果,以及特殊群体(孕妇,哺乳期女性和婴幼儿等),以及已有基础疾病人群的疫苗接种问题。
Moderna新冠疫苗试验结果报告


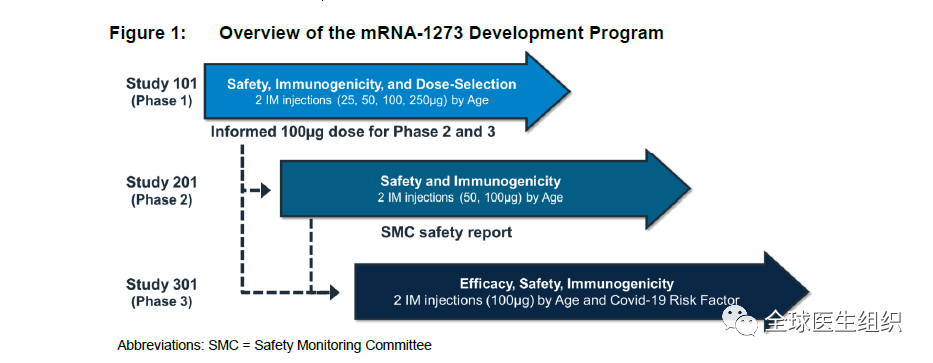

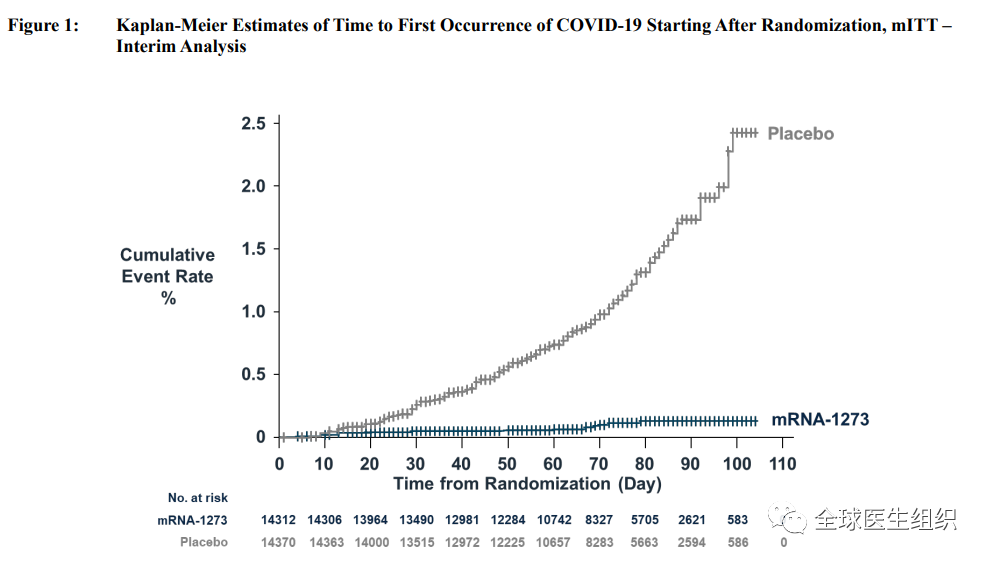


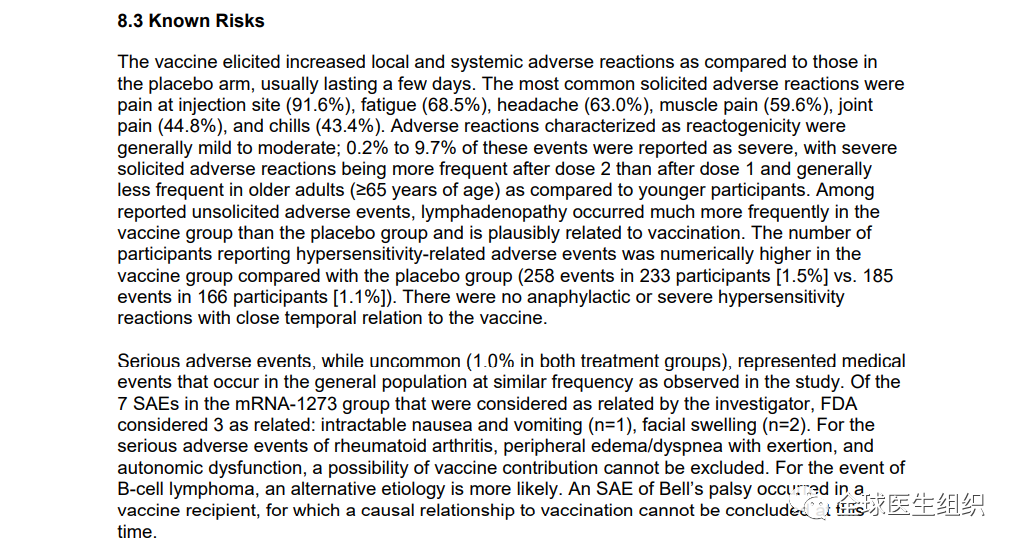
FDA-Moderna新冠疫苗审评报告







转自GlobalMD公众号:原文链接

